|
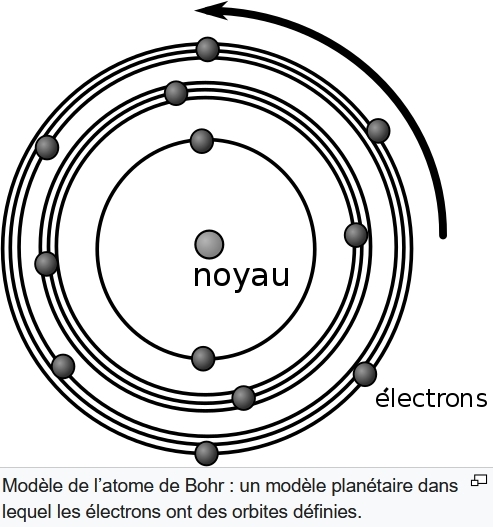
Un atome est formé d'un noyau composé de neutrons et de protons en quantité égale, autour duquel tournent des électrons sur plusieurs couches concentriques. Dans un atome stable, le nombre de protons, de neutrons et d'électrons est identique.
(Source: Wikipedia)
Le nombre de protons
détermine le matériau selon le classement du
tableau périodique des éléments. Ce tableau
(tableau de Mendeleïv), a été inventé par Dmitri
Ivanovitch Mendeleïev
Par contre, ils peuvent devenir instables si le nombre de neutrons diffère de celui des protons. On parle alors d'isotopes. L''atome a toujours le même nombre de protons (donc d'électrons) et son classement chimique dans le tableau est toujours le même. Par exemple, un atome de radium restera un atome de radium. Par contre il acquérra d'autres caractéristiques dont celle de devenir radioactif et de se désintégrer. Un atome instable se désintègre et se transforme spontanément en un autre élément en dégageant des particules (neutrons, protons, etc.) et de l'énergie sous forme de photons (lumière) et d'énergie cinétique, c'est le rayonnement ionisant. "Ionisant" car il a la particularité de modifier la matière qu'il traverse en lui enlevant des électrons .
(source: Wikipedia)
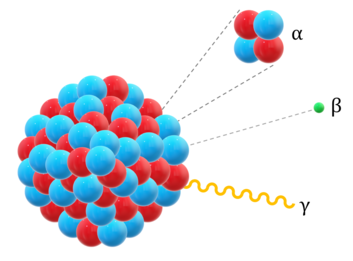
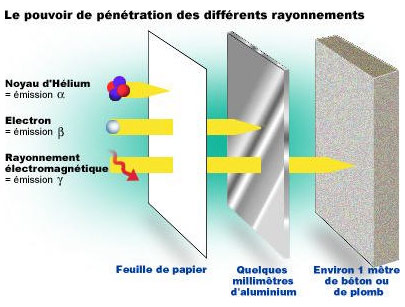
Le rayonnement se divise en 3 faisceaux qui partent dans 3 directions différentes en fonction du champ électrique ou magnétique qu'ils traversent:
La désintégration spontanée est d'autant plus grande que le nombre de protons de l'atome est grand. Ce phénomène a été découvert en 1896 par Henri Becquerel, Pierre et Marie Curie et Ernest Rutheford. Par exemple, l'uranium (92 protons) se désintègre plus que le radium (88).
Anciennes unités: R/h, Roëntgen par heure: intensité, maintenant des Sievert Dose en R (Roëntgen), maintenant des Gray
Voir cet article très intéressant sur le blog
de mon copain le Dr Goulu:
L'uranium se trouve dans la nature sous forme d'isotopes, ce qui signifie qu'il se désintègre spontanément. C'est d'ailleurs comme cela qu'on peut le découvrir, en mesurant la radioactivité du sol au moyen d'un compteur Geiger.
J'ai dit plus haut que le phénomène de la radioactivité se produit d'autant plus que l'atome a un nombre élevé de protons. C'est la raison pour laquelle on utilise des isotopes d'uranium ou de plutonium dans les centrales et les bombes atomiques.
Mais il y a encore un autre phénomène: la réaction en chaîne. Elle se produit lorsque la quantité de matière dépasse un certain volume. A ce moment-là, il y a tellement de neutrons qui sont générés que ceux-ci cassent d'autres noyaux, ce qui en ajoute encore si bien qu'on finit par atteindre ce qu'on appelle l'accident de criticité qui est un emballement, une réaction en chaîne. Le nombre de neutrons se multiplie alors jusqu'à l'infini et le matériau chauffe et finit par fondre.
Le principe d'une centrale atomique productrice d'électricité est donc de mettre en présence des barreaux de matériaux fissiles, de l'uranium en général, de façon à ce qu'ils chauffent mais n'atteignent jamais le point de non retour de la réaction en chaîne.
Par contre c'est le phénomène qu'on veut précisément obtenir pour qu'une bombe atomique explose: une réaction en chaîne qui provoque une explosion d'autant plus grande que l'emballement est rapide.
En principe, une centrale atomique ne peut pas exploser (sauf le surrégénérateur comme celui de Creys Malville par exemple) car la montée en chaleur n'est pas assez rapide. On verra plus loin comment provoquer une réaction en chaîne suffisamment rapide pour qu'une explosion ait lieu.
Au début de l'ère atomique, on appelait l'emballement thermique d'une centrale le syndrome chinois car on pensait que la fonte d'un coeur radioactif dégagerait tellement de chaleur qu'il ferait fondre tout ce qui l'environnait et s'enfoncerait dans la terre, jusqu'à réapparaître en Chine. Cela ne s'est pas vérifié, on a pu le constater lors du premier accident nucléaire de l'histoire, celui de la centrale expérimentale de Lucens, en Suisse, en 1969.
|